| Afatinib | |
|---|---|
 | |
 | |
| Nome IUPAC | |
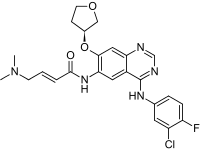
| N-[4-[(3-Chloro-4-fluorophenyl)amino]-7-[[(3S)-tetrahydro-3-furanyl]oxy]-6-quinazolinyl]-4(dimethylamino)-2-butenamide | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C24H25ClFN5O3 |
| Massa molecolare (u) | 485.937 g/mol |
| Numero CAS | |
| Numero EINECS | 810-720-4 |
| Codice ATC | L01 |
| PubChem | 10184653 |
| DrugBank | DB08916 |
| SMILES | CN(C)C\C=C\C(=O)Nc3cc1c(Nc(cc2Cl)ccc2F)ncnc1cc3OC4COCC4 |
| Dati farmacocinetici | |
| Legame proteico | 95% |
| Metabolismo | CYP non coinvolto |
| Emivita | 37 ore |
| Escrezione | Feci (85%), urina (4%) |
| Indicazioni di sicurezza | |
Afatinib, venduto tra gli altri con il marchio Giotrif, è un farmaco usato per trattare il carcinoma polmonare non a piccole cellule (NSCLC).[1] [2] Appartiene alla famiglia di farmaci inibitori della tirosina chinasi .[3] È un farmaco somministrato per vie orali.
È principalmente usato per trattare i casi di NSCLC che ospitano mutazioni nel gene del recettore del fattore di crescita epidermico (EGFR).[4]
Usi medici
Ha ricevuto l'approvazione normativa per il solo trattamento del carcinoma polmonare non a piccole cellule,[5][3][6][7] sebbene ci siano prove emergenti a supporto del suo uso benefico in altri tumori come il cancro al seno.[8]
Effetti collaterali
Gli effetti collaterali, organizzati a seconda della loro frequenza, includono:[5][6][7][9]
- Molto comune (> 10% di frequenza)
- Diarrea (>90%)
- Irritazioni/dermatiti acneformi
- Stomatiti
- Paronichia
- Moderata inappetenza
- Epistassi
- Prurito
- Pelle secca
- Comune (frequenza 1-10%)
- Disidratazione
- Alterazione del gusto
- Secchezza oculare
- Cistite
- Cheilite
- Febbre
- Naso otturato
- Bassa concentrazione di potassio nel sangue
- Congiuntivite
- ALT sopra la media
- AST sopra la media
- Eritema acrale
- Spasmi muscolari
- Disfunzione renale
- Non comune (frequenza 0,1-1%)
Meccanismo di azione
Così come lapatinib e neratinib, afatinib è un inibitore della proteina chinasi che inibisce irreversibilmente sia la chinasi del fattore di crescita epidermica umana del recettore 2 (Her2), sia quella del recettore del fattore di crescita epidermico (EGFR). Afatinib non è attivo solo contro le stesse mutazioni di EGFR che sono già bersaglio degli inibitori della tirosina-chinasi di prima generazione (TKI) come erlotinib o gefitinib, ma anche contro altre mutazioni meno comuni (contro le quali le molecole di prima generazione non hanno effetto).[10] Comunque afatinib non è attivo contro la mutazione T790M, che generalmente richiede l'utilizzo di molecole di terza generazione come osimertinib. A causa della sua attività aggiuntiva contro Her2, questa molecola è in fase di studio per il carcinoma mammario e altri tumori spinti da EGFR e Her2.[1]
Test clinici
Nel marzo 2010 è iniziato con questo farmaco uno studio di fase III su pazienti con NSCLC chiamato Lux-Lung 5 .[12] I risultati intermedi dell'autunno 2010 rivelavano un prolungamento pari al triplo nella sopravvivenza dei pazienti liberi dalla progressione della malattia, senza però incrementare la sopravvivenza globale. [13] Nel maggio 2012, lo studio di Fase IIb / III Lux-Lung 1 è giunto alla stessa conclusione.[14]
Nel gennaio 2015 uno studio di fase III su persone con NSCLC sostenne che il farmaco avesse prolungato l'aspettativa di vita nell'adenocarcinoma NSCLC in stadio IV con tumori 19-positivi di tipo Mutazione EGFR, rispetto alla tradizionale chemioterapia basata sul cisplatino, di un anno (33 mesi contro 21 mesi).[15] Lo stesso studio mostra anche la presenza di una forte attività contro le mutazioni dell'esone 18 (in particolare G719) ed è, pertanto, la terapia EGFR-TKI attualmente preferita per tali mutazioni (in particolare G719x).[16]
I risultati dei test clinici di fase II per il carcinoma mammario in cui è sovraespresso il recettore 2 del fattore di crescita epidermico umano 2 (carcinoma mammario Her2-positivo) sono stati descritti come promettenti dagli autori, con 19 su 41 pazienti che hanno tratto beneficio da afatinib.[8] Sono in corso studi di fase III col metodo doppio cieco per confermare o confutare questo risultato. Tumori al seno Her2-negativi hanno mostrato una risposta limitata o assente al farmaco.[17]
Note
- 1 2 Minkovsky N, Berezov A, BIBW-2992, a dual receptor tyrosine kinase inhibitor for the treatment of solid tumors, in Current Opinion in Investigational Drugs, vol. 9, n. 12, Dicembre 2008, pp. 1336–46, PMID 19037840.
- ↑ Afatinib, su fda.gov, US Food and Drug Administration, 12 luglio 2013.
- 1 2 GIOTRIF® Afatinib (as afatinib dimaleate), su TGA eBusiness Services, Boehringer Ingelheim Pty Limited, 7 novembre 2013. URL consultato il 28 gennaio 2014.
- ↑ Role of afatinib in the treatment of advanced lung squamous cell carcinoma, in Clinical Pharmacology, vol. 9, 2017, pp. 147–157, DOI:10.2147/CPAA.S112715, PMID 29225480.
- 1 2 GILOTRIF (afatinib) tablet, film coated [Boehringer Ingelheim Pharmaceuticals, Inc.], su DailyMed, Boehringer Ingelheim Pharmaceuticals, Inc., Novembre 2013. URL consultato il 28 gennaio 2014.
- 1 2 Giotrif 20 mg film-coated tablets – Summary of Product Characteristics (SPC), su electronic Medicines Compendium, Boehringer Ingelheim Limited, 20 gennaio 2014. URL consultato il 28 gennaio 2014.
- 1 2 Giotrif : EPAR -Product Information (PDF), su European Medicines Agency, Boehringer Ingelheim International GmbH, 16 ottobre 2013. URL consultato il 28 gennaio 2014.
- 1 2 Lin NU, Winer EP, Wheatley D, Carey LA, Houston S, Mendelson D, et al., A phase II study of afatinib (BIBW 2992), an irreversible ErbB family blocker, in patients with HER2-positive metastatic breast cancer progressing after trastuzumab, in Breast Cancer Research and Treatment, vol. 133, n. 3, Giugno 2012, pp. 1057–65, DOI:10.1007/s10549-012-2003-y, PMC 3387495, PMID 22418700.
- ↑ Gilotrif (afatinib) dosing, indications, interactions, adverse effects, and more, su Medscape Reference, WebMD. URL consultato il 28 gennaio 2014.
- ↑ BIBW2992, an irreversible EGFR/HER2 inhibitor highly effective in preclinical lung cancer models, in Oncogene, vol. 27, n. 34, Agosto 2008, pp. 4702–11, DOI:10.1038/onc.2008.109, PMID 18408761.
- ↑ Schubert-Zsilavecz, M, Wurglics, M, Neue Arzneimittel Frühjahr 2013. (DE)
- ↑ Clinical trial number NCT01085136 for "LUX-Lung 5: BIBW 2992 Plus Weekly Paclitaxel Versus Investigator's Choice of Single Agent Chemotherapy Following BIBW 2992 Monotherapy in Non-small Cell Lung Cancer Patients Failing Erlotinib or Gefitinib" at ClinicalTrials.gov
- ↑ Afatinib (BIBW 2992*) Triples Progression Free Survival in Phase III Study in Lung Cancer Patients, su businesswire.com, BusinessWire, 11 ottobre 2010.
- ↑ Miller VA, Hirsh V, Cadranel J, Chen YM, Park K, Kim SW, et al., Afatinib versus placebo for patients with advanced, metastatic non-small-cell lung cancer after failure of erlotinib, gefitinib, or both, and one or two lines of chemotherapy (LUX-Lung 1): a phase 2b/3 randomised trial, in The Lancet. Oncology, vol. 13, n. 5, Maggio 2012, pp. 528–38, DOI:10.1016/S1470-2045(12)70087-6, PMID 22452896.
- ↑ Afatinib versus cisplatin-based chemotherapy for EGFR mutation-positive lung adenocarcinoma (LUX-Lung 3 and LUX-Lung 6): analysis of overall survival data from two randomised, phase 3 trials, in The Lancet. Oncology, vol. 16, n. 2, February 2015, pp. 141–51, DOI:10.1016/s1470-2045(14)71173-8, PMID 25589191.
- ↑ EGFR Exon 18 Mutations in Lung Cancer: Molecular Predictors of Augmented Sensitivity to Afatinib or Neratinib as Compared with First- or Third-Generation TKIs, in Clinical Cancer Research, vol. 21, n. 23, Dicembre 2015, pp. 5305–13, DOI:10.1158/1078-0432.CCR-15-1046, PMID 26206867.
- ↑ Schuler M, Awada A, Harter P, Canon JL, Possinger K, Schmidt M, et al., A phase II trial to assess efficacy and safety of afatinib in extensively pretreated patients with HER2-negative metastatic breast cancer, vol. 134, n. 3, Agosto 2012, pp. 1149–59, DOI:10.1007/s10549-012-2126-1, PMC 3409367, PMID 22763464.
Altri progetti
 Wikimedia Commons contiene immagini o altri file su Afatinib
Wikimedia Commons contiene immagini o altri file su Afatinib
