| Canagliflozin | |
|---|---|
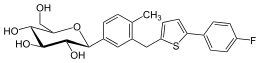 | |
| Nome IUPAC | |
| (2S,3R,4R,5S,6R)-2-{3-[5-[4-Fluoro-fenil)-tiofen-2-ilmetil]-4-metil-fenil}-6-idrossimetil-tetraidro-piran-3,4,5-triolo | |
| Nomi alternativi | |
| JNJ-24831754; TA-7284; (1S)-1,5-anhydro-1-C-[3- [[5-(4-fluorofenil)-2-tienil]metil]-4-metilfenil]-D-glucitolo | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C24H25FO5S |
| Massa molecolare (u) | 444,52 |
| Numero CAS | |
| Numero EINECS | 695-192-1 |
| PubChem | 24812758 |
| DrugBank | DB08907 |
| SMILES | CC1=C(C=C(C=C1)C2C(C(C(C(O2)CO)O)O)O)CC3=CC=C(S3)C4=CC=C(C=C4)F |
| Dati farmacologici | |
| Categoria farmacoterapeutica | Antidiabetici |
| Modalità di somministrazione | Orale |
| Dati farmacocinetici | |
| Biodisponibilità | 65% |
| Indicazioni di sicurezza | |
Il Canagliflozin (commercializzato negli Stati Uniti d'America con il nome Invokana) è un farmaco per il trattamento del diabete mellito di tipo 2.[1][2] È stato sviluppato da Mitsubishi Tanabe Pharma ed è commercializzato sotto licenza da Janssen, una divisione della Johnson & Johnson.[3]
Nel marzo del 2013, il canagliflozin è diventato il primo inibitore del SGLT2 ad essere approvato negli Stati Uniti.[4]
Farmacodinamica
Il Canagliflozin è un inibitore del trasportatore di membrana sottotipo 2 della proteina di trasporto selettivo del sodio glucosio (SGLT2), che è responsabile per almeno il 90% del riassorbimento del glucosio nel rene.[5] Esso blocca il riassorbimento del glucosio dal rene, aumentando l'escrezione di glucosio e abbassandone quindi i livelli ematici nelle persone affette da diabete.[6]
Indicazioni
Il canagliflozin è stato studiato come monoterapia o in combinazione con altre terapie del diabete tipo 2 quali metformina, sulfaniluree, pioglitazone e insulina. Il farmaco non deve essere usato per trattare le persone con chetoacidosi diabetica o in quelle con insufficienza renale grave, malattia renale cronica terminale e nei pazienti in dialisi.
Effetti avversi
Gli effetti avversi più comuni del farmaco sono infezione vaginale e infezione delle vie urinarie da candida nel 10% dei pazienti.[7] Inoltre l'effetto diuretico del farmaco può determinare, in alcuni casi, una riduzione del volume intravascolare che porta a ipotensione posturale o ortostatica. Questo può causare vertigini o lipotimia (svenimenti), più comuni nei primi tre mesi di terapia.[8] Sono segnalati anche casi di gangrena di Fournier (fascite necrotizzante del perineo).
Note
- ↑ New J&J diabetes drug effective in mid-stage study Archiviato il 24 settembre 2015 in Internet Archive., Jun 26, 2010
- ↑ Edward C. Chao, Canagliflozin, in Drugs of the Future, vol. 36, n. 5, 2011, pp. 351–357, DOI:10.1358/dof.2011.36.5.1590789.
- ↑ (EN) First Results from Phase 3 CANVAS Trial Show Canagliflozin as Add-on Therapy to Insulin Lowered Blood Sugar Levels in Patients with Type 2 Diabetes at an Elevated Risk for Cardiovascular Disease (NYSE:JNJ), su investor.jnj.com (archiviato dall'url originale il 13 marzo 2013).
- ↑ (EN) FDA approves Invokana to treat type 2 diabetes, su fda.gov.
- ↑ Prous Science: Molecule of the Month November 2007
- ↑ (EN) FDA Advisory Committee Recommends Approval of Canagliflozin for Treatment of Adults with Type 2 Diabetes, su jnj.com (archiviato dall'url originale il 3 aprile 2013).
- ↑ SA. Nisly, DM. Kolanczyk; AM. Walton, Canagliflozin, a new sodium-glucose cotransporter 2 inhibitor, in the treatment of diabetes., in Am J Health Syst Pharm, vol. 70, n. 4, febbraio 2013, pp. 311-9, DOI:10.2146/ajhp110514, PMID 23370138.
- ↑ K. Stenlöf, WT. Cefalu; KA. Kim; M. Alba; K. Usiskin; C. Tong; W. Canovatchel; G. Meininger, Efficacy and safety of canagliflozin monotherapy in subjects with type 2 diabetes mellitus inadequately controlled with diet and exercise., in Diabetes Obes Metab, vol. 15, n. 4, aprile 2013, pp. 372-82, DOI:10.1111/dom.12054, PMID 23279307.
Bibliografia
- C. Clar, JA. Gill; R. Court; N. Waugh, Systematic review of SGLT2 receptor inhibitors in dual or triple therapy in type 2 diabetes., in BMJ Open, vol. 2, n. 5, 2012, DOI:10.1136/bmjopen-2012-001007, PMID 23087012.
- Y. Liang, K. Arakawa; K. Ueta; Y. Matsushita; C. Kuriyama; T. Martin; F. Du; Y. Liu; J. Xu; B. Conway; J. Conway, Effect of canagliflozin on renal threshold for glucose, glycemia, and body weight in normal and diabetic animal models., in PLoS One, vol. 7, n. 2, 2012, pp. e30555, DOI:10.1371/journal.pone.0030555, PMID 22355316.
Voci correlate
Altri progetti
 Wikimedia Commons contiene immagini o altri file su Canagliflozin
Wikimedia Commons contiene immagini o altri file su Canagliflozin